에이비엘바이오, 1년 전 1400억 CPS 투자자 '8000억' 잭팟
인터베스트 등 전환가액 대비 7배 차익, 보호예수 해제에도 장기 성장 베팅
에이비엘바이오가 올해만 두건의 기술이전 성과를 올리며 시가총액이 10조원에 다다를 정도로 급등했다. 이에 작년 1400억원 규모의 유상증자에 참여한 투자자들의 수익구조에도 세간의 관심이 몰린다. 대략 현재 8000억원대의 잠재 차익을 기록한 것으로 추정된다.
투자자의 기대는 올해에 그치지지 않는다. 에이비엘바이오는 후속 파이프라인의 사업화 성과와 함께 투자자들과의 장기적인 투자 관계를 이어간다. 이중항체-약물접합체(ADC) 본임상 진입과 컨퍼스테라퓨틱스의 ABL001 가속 신약 허가 등에 대한 성과에 주목한다.
◇잇단 BBB 셔틀 플랫폼 L/O 성과, 시총 9조 돌파
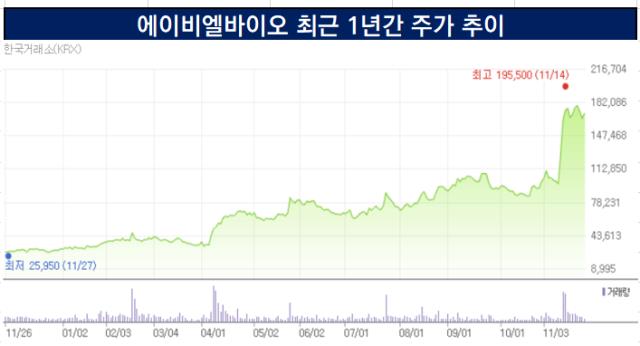
에이비엘바이오의 밸류는 올해 뇌혈관장벽(BBB) 셔틀 플랫폼 '그랩바디-B' 기반 기술이전 계약을 잇따라 체결하며 급격히 성장했다. 이달 25일 종가는 16만6000원으로 시가총액은 9조원을 훌쩍 넘어섰다.
올해 4월 7일 GSK와 맺은 그랩바디-B 기술이전 계약이 시작점이다. 에이비엘바이오는 GSK와 복수의 프로그램에 대한 개발, 허가 및 상업화 마일스톤을 포함해 약 20억6300만 파운드, 한화 약 3조8519억원 규모 계약을 체결했다.
대규모 딜에 힘입어 에이비엘바이오의 몸값은 크게 올랐다. 기술이전 계약 직전 거래일인 4일 시가총액은 1조6524억원이었으나 GSK와의 거래가 공개된 당일 2조원대에 진입했다. 같은 기간 주가는 3만4050원에서 4만4250원으로 상승했다.
이후 그랩바디-B를 기반으로 또 한 번의 글로벌 빅딜을 성사시켰다. 에이비엘바이오는 이달 12일 일라이릴리와 신약개발을 위한 그랩바디 플랫폼 기술이전 및 공동 연구개발 계약을 체결했다. 총 계약 규모는 26억200만달러, 한화 약 3조8072억원이다.
에이비엘바이오의 주가가 빠르게 상승하자 작년 7월 1400억원 규모의 유상증자에 참여한 투자자들의 차익이 주목받고 있다. 투자자는 한국산업은행, 에이티넘인베스트먼트, 인터베스트, 하나벤쳐스, 하나증권, 컴퍼니케이파트너스 등이다.
당시 에이비엘바이오는 보통주가 아닌 전환우선주(CPS)를 발행했다. CPS는 보통주로 전환할 경우 자본이득을 기대할 수 있고 우선주인 만큼 배당 우선권을 갖는 점이 장점으로 꼽힌다. 에이비엘바이오는 배당을 실시하지 않지만 투자자들은 주가 상승에 따른 자본이득을 기대하며 유상증자에 참여했다.
현재까지 투자자들이 유상증자 참여로 얻은 차익은 8192억원으로 추산된다. 해당 투자자들은 올해 7월 전환청구기간이 개시되자 CPS 전량을 보통주로 전환했다. 전환가액은 2만4229원이며 보통주로 557만8196주가 전환됐다.
25일 종가 16만6000원을 기준으로 계산하면 전환가액 대비 약 7배에 달하는 이득을 얻은 상태다. 투자금은 1351억원, 보통주의 현재 주식 가치는 9544억원으로 추산된다. 매도를 진행할 시 오버행도 우려될 수 있는 구조지만 현재 투자자들은 보통주 형태로 주식을 보유하고 있다.
◇투자자 이해관계 계속 유지, 상업화·본임상 등 모멘텀 겸비
에이비엘바이오는 앞서 오버행에 대한 우려도 잠재웠다. 보통주 전환 당시 이상훈 에이비엘바이오 대표가 기업설명회에서 '투자자들이 1년 후 회수보다 장기적 성장을 기대하고 있다'고 강조한 게 주된 근거다. 현재까지도 매도 없이 투자 관계가 이어지고 있다는 설명이다.
에이비엘바이오 관계자는 "기업설명회 때 전달했듯이 여전히 투자자들과는 관계를 유지해나가는 중"이라며 "추가 유상증자 계획은 없으며 현재 투자자들과 이해관계를 이어나갈 예정"이라고 말했다.
투자자 입장에서는 내년에도 기대되는 모멘텀이 있다. 두 건의 딜을 성사시킨 에이비엘바이오는 다음 스텝으로 로열티를 통한 자체 수익모델 구축을 목표하고 있다. 현재 미국 파트너사 컨퍼스테라퓨틱스와 함께 개발 중인 담도암 치료제 'ABL001' 승인에 집중할 계획이다.
ABL001은 현재 미국에서 임상 2/3상을 진행 중이다. 허가를 목표로 하는 시점은 내년 말로 상업화 단계까지 도달할 경우 연 500억원 수준의 로열티를 꾸준히 벌어들일 수 있을 것으로 추정된다.

내년 1분기에도 기대할 수 있는 소식이 있다. 에이비엘바이오는 이중항체 ADC 파이프라인 ABL206과 ABL209를 보유하고 있다. 내년 1분기 미국 식품의약국(FDA)에 임상시험계획(IND)을 신청한다. 이후 미국 이중항체 ADC 전문 자회사인 네옥바이오가 본임상을 이끈다. 향후 네옥바이오의 성과가 에이비엘바이오의 주가로 이어질 수 있는 구조다.
에이비엘바이오 관계자는 "이중항체 ADC의 임상 1상 IND까지는 에이비엘바이오에서 진행하고 이후 네옥바이오가 개발을 담당한다"며 "내년에 임상 1상에 들어가면 해당 내용을 내년 4월 미국암학회(AACR)에서 공개할 예정"이라고 말했다.
투자자의 기대는 올해에 그치지지 않는다. 에이비엘바이오는 후속 파이프라인의 사업화 성과와 함께 투자자들과의 장기적인 투자 관계를 이어간다. 이중항체-약물접합체(ADC) 본임상 진입과 컨퍼스테라퓨틱스의 ABL001 가속 신약 허가 등에 대한 성과에 주목한다.
◇잇단 BBB 셔틀 플랫폼 L/O 성과, 시총 9조 돌파
에이비엘바이오의 밸류는 올해 뇌혈관장벽(BBB) 셔틀 플랫폼 '그랩바디-B' 기반 기술이전 계약을 잇따라 체결하며 급격히 성장했다. 이달 25일 종가는 16만6000원으로 시가총액은 9조원을 훌쩍 넘어섰다.

올해 4월 7일 GSK와 맺은 그랩바디-B 기술이전 계약이 시작점이다. 에이비엘바이오는 GSK와 복수의 프로그램에 대한 개발, 허가 및 상업화 마일스톤을 포함해 약 20억6300만 파운드, 한화 약 3조8519억원 규모 계약을 체결했다.
대규모 딜에 힘입어 에이비엘바이오의 몸값은 크게 올랐다. 기술이전 계약 직전 거래일인 4일 시가총액은 1조6524억원이었으나 GSK와의 거래가 공개된 당일 2조원대에 진입했다. 같은 기간 주가는 3만4050원에서 4만4250원으로 상승했다.
이후 그랩바디-B를 기반으로 또 한 번의 글로벌 빅딜을 성사시켰다. 에이비엘바이오는 이달 12일 일라이릴리와 신약개발을 위한 그랩바디 플랫폼 기술이전 및 공동 연구개발 계약을 체결했다. 총 계약 규모는 26억200만달러, 한화 약 3조8072억원이다.
에이비엘바이오의 주가가 빠르게 상승하자 작년 7월 1400억원 규모의 유상증자에 참여한 투자자들의 차익이 주목받고 있다. 투자자는 한국산업은행, 에이티넘인베스트먼트, 인터베스트, 하나벤쳐스, 하나증권, 컴퍼니케이파트너스 등이다.
당시 에이비엘바이오는 보통주가 아닌 전환우선주(CPS)를 발행했다. CPS는 보통주로 전환할 경우 자본이득을 기대할 수 있고 우선주인 만큼 배당 우선권을 갖는 점이 장점으로 꼽힌다. 에이비엘바이오는 배당을 실시하지 않지만 투자자들은 주가 상승에 따른 자본이득을 기대하며 유상증자에 참여했다.
현재까지 투자자들이 유상증자 참여로 얻은 차익은 8192억원으로 추산된다. 해당 투자자들은 올해 7월 전환청구기간이 개시되자 CPS 전량을 보통주로 전환했다. 전환가액은 2만4229원이며 보통주로 557만8196주가 전환됐다.
25일 종가 16만6000원을 기준으로 계산하면 전환가액 대비 약 7배에 달하는 이득을 얻은 상태다. 투자금은 1351억원, 보통주의 현재 주식 가치는 9544억원으로 추산된다. 매도를 진행할 시 오버행도 우려될 수 있는 구조지만 현재 투자자들은 보통주 형태로 주식을 보유하고 있다.
◇투자자 이해관계 계속 유지, 상업화·본임상 등 모멘텀 겸비
에이비엘바이오는 앞서 오버행에 대한 우려도 잠재웠다. 보통주 전환 당시 이상훈 에이비엘바이오 대표가 기업설명회에서 '투자자들이 1년 후 회수보다 장기적 성장을 기대하고 있다'고 강조한 게 주된 근거다. 현재까지도 매도 없이 투자 관계가 이어지고 있다는 설명이다.
에이비엘바이오 관계자는 "기업설명회 때 전달했듯이 여전히 투자자들과는 관계를 유지해나가는 중"이라며 "추가 유상증자 계획은 없으며 현재 투자자들과 이해관계를 이어나갈 예정"이라고 말했다.
투자자 입장에서는 내년에도 기대되는 모멘텀이 있다. 두 건의 딜을 성사시킨 에이비엘바이오는 다음 스텝으로 로열티를 통한 자체 수익모델 구축을 목표하고 있다. 현재 미국 파트너사 컨퍼스테라퓨틱스와 함께 개발 중인 담도암 치료제 'ABL001' 승인에 집중할 계획이다.
ABL001은 현재 미국에서 임상 2/3상을 진행 중이다. 허가를 목표로 하는 시점은 내년 말로 상업화 단계까지 도달할 경우 연 500억원 수준의 로열티를 꾸준히 벌어들일 수 있을 것으로 추정된다.

내년 1분기에도 기대할 수 있는 소식이 있다. 에이비엘바이오는 이중항체 ADC 파이프라인 ABL206과 ABL209를 보유하고 있다. 내년 1분기 미국 식품의약국(FDA)에 임상시험계획(IND)을 신청한다. 이후 미국 이중항체 ADC 전문 자회사인 네옥바이오가 본임상을 이끈다. 향후 네옥바이오의 성과가 에이비엘바이오의 주가로 이어질 수 있는 구조다.
에이비엘바이오 관계자는 "이중항체 ADC의 임상 1상 IND까지는 에이비엘바이오에서 진행하고 이후 네옥바이오가 개발을 담당한다"며 "내년에 임상 1상에 들어가면 해당 내용을 내년 4월 미국암학회(AACR)에서 공개할 예정"이라고 말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >


